Présent et avenir de la prise en charge des céphalées primaires
Présent et
avenir de la prise en charge des céphalées primaires.
Migraine et
algie vasculaire de la face
Christian Lucas
Centre d’Evaluation et de Traitement de la
Douleur, service de Neurochirurgie, Hôpital Salengro, CHRU de Lille. christian.lucas@chru-lille.fr
La prise en charge de la migraine
repose pour les traitements de crise sur les AINS et les triptans1.
Pour les traitements de fond nous disposons de nombreuses molécules non
spécifiques (béta-bloquants, tricycliques, certains anti-épileptiques…) mais
qui ne sont pas dépourvus d’effets secondaires1. Il en est de même
pour l’algie vasculaire de la face (AVF), beaucoup plus rare que la migraine,
mais particulièrement invalidante. Les traitements de crise de l’AVF reposent
sur le sumatriptan injectable 6 mg en SC et/ou l’oxygène à 12 à 15l/min pendant
20 minutes au masque à haute concentration. Le traitement de fond de 1ère
ligne repose sur le vérapamil à la posologie minimale de 360 mg/j2.
Des
traitements de fond spécifiques en accord avec la physiopathologie des
céphalées primaires sont donc souhaitables…
Les nouveaux
traitements médicamenteux de fond en développement : Anticorps
monoclonaux anti-CGRP (Calcitonin Gene Releated Peptide)
Il s’agit d’une nouvelle génération de traitement de fond en phase de
développement (phases III en cours).
Le CGRP est un neuromédiateur, composé de 37 acides aminés, distribué
dans l’ensemble du système nerveux central et périphérique, ayant, entre
autres, un rôle pro-inflammatoire et algogène et qui est largué au pourtour des
vaisseaux méningés lors de la crise de migraine (et également lors de la crise
d’algie vasculaire de la face)3-4. Le taux de CGRP est élevé dans le
sang veineux (veine jugulaire) au décours d’une crise migraineuse et également
en dehors des crises5-6. Quatre laboratoires pharmaceutiques (Alder,
Lilly, Novartis et Teva) ont développé des anticorps monoclonaux humanisés ou
totalement humanisés pour bloquer l’action du CGRP. La population cible des
essais sont les migraineux épisodiques à haute fréquence en échec de 2 à 4
traitements de fond traditionnels de la migraine les patients migraineux
chroniques (ayant au moins 15 jours de céphalées par mois dont 8 crises
migraineuses et ce depuis au moins 3 mois) et également en échec thérapeutique
et les patients ayant une AVF7-10. Les anticorps monoclonaux
anti-CGRP sont administrés une fois par mois par voie parentérale
(essentiellement en sous-cutané) et s’avèrent, pour le moment, avec les
résultats dont on dispose, efficaces (et ce rapidement entre 7 et 14 jours) et
bien tolérés. Ils vont, probablement, révolutionner la prise en charge des
migraineux les plus sévères et des patients ayant une AVF.
Conflits d’intérêts : le Dr Lucas a des missions de conseils scientifiques pour les
laboratoires Lilly, Novartis, Sanofi, Teva.
Références
1.
Lanteri-Minet
M, Valade D, Geraud G, Lucas C, Donnet A. Revised
French guidelines for the diagnosis and management of migraine in adults and
children. J Headache Pain. 2014;
15(1):2.
2. Donnet A, Demarquay G, Ducros A, Geraud G, Giraud P, Guegan-Massardier E, Lucas C, Navez M, Valade D Lanteri-Minet M. French guidelines for
diagnosis and treatment of cluster headache (French Headache Society). Rev Neurol. 2014 Jun 17.
3. Russo
AF. Calcitonin gene-related peptide (CGRP): a new target for migraine. Annu Rev
Pharmacol Toxicol 2015; 55: 533-52.
4.
Ashina M, Bendtsen L, Jensen R et al. Evidence
for increased plasma levels of calcitonin gene-related peptide in migraine
outside of attacks. Pain
2000 ; 86: 133-8.
5. Cernuda-Morollon E, Larrosa D, Ramon C et al. Interictal
increase of CGRP levels in peripheral blood as a biomarker for chronic
migraine. Neurology 2013; 81: 1191-6.
6. Bigal
ME, Dodick DW, Rapoport AM et al. Safety, tolerability, and efficacy of
TEV48125 for preventive treatment of high-frequency episodic migraine: a
multicenter, randomized, double-blind, placebo-controlled, phase 2b study.
Lancet Neurol 2015; 14: 1081-9.
7. Dodick
DW, Goadsby PJ, Spierings ELH et al. Safety and efficacy of LY2951742, a
monoclonal antibody to calcitonin gene-related peptide, for the prevention of
migraine: a phase 2, randomized, double-blind, placebo-controlled study. Lancet
Neurol 2014; 13: 885-92.
8. Sun
H, Dodick DW, Silberstein S et al. Safety and efficacy of AMG 334 for
prevention of episodic: a randomized, double-blind, placebo-controlled, phase 2
trial. Lancet Neurol 2016; 15: 382-90.
9. Dodick
DW, Goadsby PJ, Silbertein SD et al. Safety and efficacy of ALD403, an antibody
to calcitonin gene-related peptide, for the prevention of frequent episodic
migraine: a randomised, double-blind, placebo-controlled, exploratory phase 2
trial. Lancet Neurol 2014; 13: 1100-7.
10. Bigal
ME, Edvinsson L, Rapoport AM et al. Safety, tolerability, and efficacy of
TEV48125 for preventive treatment of chronic migraine: a multicenter,
randomized, double-blind, placebo-controlled, phase 2b study. Lancet Neurol
2015; 14: 1091-100.
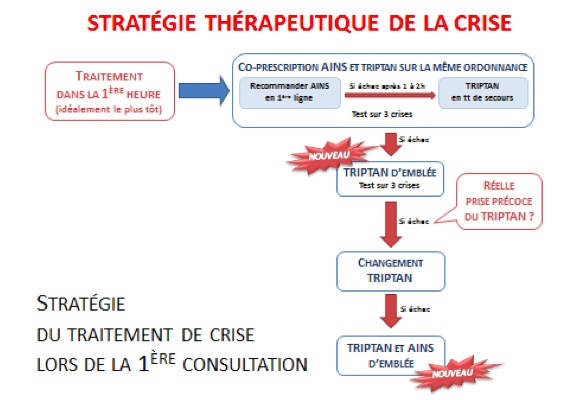
Figure : stratégie thérapeutique du traitement de crise lors de la 1ère consultation dédiée à la migraine