Diabétologie : matériel, instauration de l'insulinothérapie
Docteur Dominique BOUTE
29 bis rue Sadi Carnot
59280 ARMENTIERES
Le diabète de type 2 est plus que jamais un problème courant pour le médecin-traitant tant l’accroissement de cette affection se fait de façon épidémique sur l’ensemble de la planète. La prévalence du diabète est de 3.8 % et augmente de 4.2 % par an en France. Ceci est sans compter le nombre de patients diabétiques méconnus, une estimation porte le nombre de patients diabétiques en France en 2007 à plus de 2 500 000.
Le problème de cette affection est son évolution à bas bruit qui expose le patient à de multiples complications et une mortalité deux fois plus élevée par rapport aux sujets non diabétiques. Améliorer la prise en charge du patient diabétique de type 2 est un réel enjeu de santé publique.
L’histoire naturelle du diabète de type 2
L’histoire naturelle du diabète de type 2 commence par l’insulino-résistance qui s’installe à l’occasion d’une prédisposition héréditaire associée à des facteurs environnementaux. L’âge, la sédentarité, le surpoids en particulier dans sa répartition abdominale, les composantes émotionnelles liées au stress, favorisent l’apparition du syndrome d’insulino-résistance et ses perturbations métaboliques et viscérales. L’ensemble de ces anomalies est regroupé aujourd’hui sous le terme de syndrome métabolique associant à des degrés divers une répartition abdominale des graisses (évaluée par le tour de taille), un trouble de la tolérance glucidique (retrouvé par une glycémie à jeun entre 1.10 et 1.27 g/l), des perturbations lipidiques dont l’hypertriglycéridémie et la baisse du cholestérol HDL, une hypertension artérielle et d’autres perturbations comme la stéatose hépatique, l’hyperuricémie, l’augmentation de la micro-albuminurie, etc. L’augmentation de la fréquence de l’obésité dans nos populations favorise ce syndrome métabolique qui s’installe parfois à un très jeune âge et influence ainsi la progression du risque de diabète de type 2.
Tant que le pancréas compense cette résistance à l’insuline en augmentant sa production d’insuline, la glycorégulation reste en-dessous du seuil de diabète. L’apparition du diabète est ainsi liée à cette incapacité pour le pancréas à compenser l’insulino-résistance conduisant à une majoration de troubles de la glycorégulation. On parle ainsi de diabète lorsque la glycémie à jeun contrôlée à deux reprises est au-delà de 1.27 g/l ou lorsque les glycémies post-prandiales sont au-dessus de 2 g/l.
L’apparition d’un diabète est donc toujours le témoin d’une diminution des capacités d’insulino-secrétion. Ceci a en particulier été bien démontré par l’étude UKPDS objectivant que l’aggravation progressive de la maladie diabétique est en relation avec une diminution de la sécrétion d’insuline. Parmi les facteurs qui favorisent cette altération de l’insulino-secrétion, on peut souligner le rôle de la glucotoxocité, c’est-à-dire l’impact délétère de l’hyperglycémie chronique sur le fonctionnement de la cellule B de Langherans. Dans le cadre du syndrome d’insulino-résistance, une anomalie de la répartition des triglycérides est également objectivée avec une infiltration graisseuse y compris retrouvée au niveau pancréatique évoquant également un processus de l’hypotoxicité. Le turn-over accéléré des acides gras entre dans ce mécanisme pathologique.
Cette toxicité « métabolique » pour le pancréas peut évoluer vers une réelle réduction de la masse insulino-secrétrice par apoptose des cellules bêta.
La compréhension de l’histoire naturelle de la maladie diabétique dans le diabète de type 2 permet de mieux comprendre les enjeux de la stratégie thérapeutique comme le montrent aujourd’hui les recommandations de prise en charge. L’exigence de contrôles glycémiques stricts au début du diabète pourrait peut-être permettre de préserver le plus longtemps possible un potentiel d’insulino-secrétion qui évite l’aggravation de la maladie diabétique. Toutefois avec le temps les mesures pour préserver cette insulino-sécrétion diminuent et une insulinothérapie peut devenir indispensable.
La stratégie thérapeutique
Traiter le diabète c’est éviter l’apparition des complications liées à ce diabète. Cette prise en charge doit s’intégrer dans une stratégie globale orientée sur l’amélioration de l’ensemble des facteurs de risque du patient. Elle intègre souvent un lourd traitement car outre le contrôle glycémique, le contrôle tensionnel, lipidique, anti-plaquettaire est souvent indispensable chez les patients qui ont parfois déjà un passé cardiovasculaire. Cette prise en charge intègre aussi des mesures de contrôle des facteurs environnementaux, diététique, activité physique, sevrage tabagique… Le contrôle pondéral est également un enjeu dans la prise en charge du diabète. L’ensemble de ces facteurs montre que la motivation du patient est un élément clé à la réussite et la prise en charge du diabète entre pleinement dans le champ de l’éducation thérapeutique du patient. L’approche motivationnelle est fondamentale dès le début du diabète.
La stratégie thérapeutique du diabète de type 2 est en effet progressive et les recommandations de prise en charge constituent un guide permettant de rechercher à chaque étape une optimisation du contrôle glycémique. Tout au long de cette stratégie le contrôle des mesures diététiques et la promotion de l’activité physique sont indispensables. Bien entendu ces mesures seront adaptées aux capacités du patient. Les premières étapes thérapeutiques reposent sur les traitements oraux que l’on peut diviser aujourd’hui en trois grandes classes :
- les médicaments favorisant l’utilisation du glucose : la metformine et les glitazones
- les médicaments réduisant l’absorption du glucose : l’acarbose
- les médicaments influençant l’insulinosécrétion :
o Les incrétines (inhibiteurs de la DPP4) : ces médicaments prolongent l’effet des hormones entérodigestives (GLP1, GIP) qui sensibilisent la réponse insulinosécrétrice au stimulus « glucose » et diminuent la sécrétion de Glucagon.
o Les sulfamides hypoglycémiants et les glinides stimulant l’insulinosécrétion.
Les traitements injectables du diabète de type 2 se sont élargis avec la mise à disposition des analogues du GLP1. Ils rejoignent les inhibiteurs de la DPP4 pour former la nouvelle classe des incrétines avec une action centrale sur le contrôle de la satiété.
L’insulinothérapie dans le diabète de type 2 s’intègre dans la stratégie thérapeutique du diabète de type 2. Elle est indiquée lorsque le diabète reste insuffisamment contrôlé malgré une bithérapie orale maximale comportant un biguanide et un sulfamide ou un traitement triple. Le niveau d’HbA1c retenu pour envisager une insulinothérapie est de 8%.
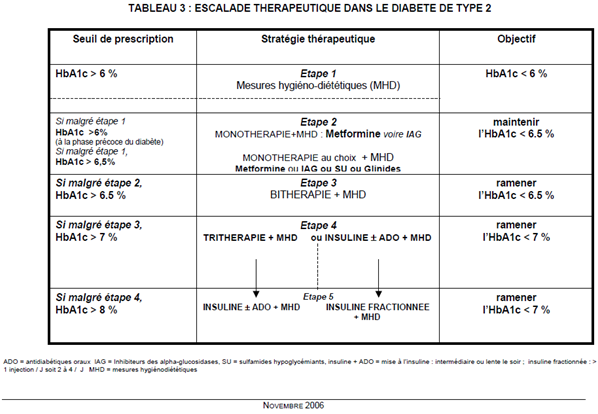
La stratégie thérapeutique a été clairement définie dans les recommandations de l’HAS de 2006 dont le tableau ci- rappelle les grandes étapes.
Ces recommandations n’intègrent pas la nouvelle classe des incrétines que l’on peut schématiquement positionner pour les inhibiteurs de la DPP4 à un stade précoce en bithérapie en association avec la metformine (Etape 3)et pour les analogues du GLP1à un stade plus tardif avant d’envisager l’insulinothérapie (Etape 4). Cette stratégie mérite d’être définie par de nouvelles recommandations professionnelles.
Il n’en reste pas moins que la stratégie thérapeutique du diabète doit être envisagée d’une façon progressive dans le temps avec une exigence à chaque étape d’optimisation du contrôle glycémique. C’est l’avantage des recommandations de nous pousser en tant que médecin vers cette exigence.
L’insulinothérapie dans le diabète de type 2 en pratique
Nous envisageons la première étape de cette mise sous insuline avec maintien de la metformine et de l’insulinosécréteur (sulfamides ou glinides) et adjonction d’une insuline basale.
Pour cette étape, nous envisageons les analogues lents comme l’insuline Detemir (Levemir®) ou l’insuline Glargine (Lantus®).
La finalité de ce schéma est de contrôler le niveau glycémique à jeun par la Metformine et l’augmentation du niveau de base d’insuline permettant de normaliser la glycémie à jeun et de maintenir la stimulation de la sécrétion endogène d’insuline en particulier pour la période post prandiale par les insulinosécréteurs.
Cette instauration de l’insulinothérapie peut aisément se faire en ambulatoire chez un patient motivé.
Différentes étapes sont nécessaires (En absence d’accords professionnels, la démarche proposée reflète l’opinion de l’auteur):
1) Optimisation du traitement, autosurveillance et préparation du patient
La mise sous insuline en ambulatoire ne peut s’envisager que chez un patient maîtrisant l’autosurveillance. Ceci est dans la grande majorité des cas installé en particulier avec la mise en place d’un insulinosécréteur.
La motivation du patient est un autre point majeur. Sa résistance est souvent le reflet de croyances, d’idées reçues, d’angoisse… L’annonce de la mise sous insuline est parfois vécue comme un réel traumatisme. L’écoute active et l’abord motivationnel prennent une place majeure dans cette mise en place. C’est l’occasion de revoir la prise en charge globale du patient et même d’obtenir une meilleure adhésion aux modifications diététiques et environnementales, d’optimiser le traitement tout en se méfiant de ne pas faire passer l’insulinothérapie comme une « sanction thérapeutique ».
Il est souhaitable d’envisager la mise sous insuline lors d’une consultation spécifique. La mise sous insulinothérapie dans le diabète de type 2 ne se fait pas dans l’urgence mais dans le cadre d’une stratégie prévue de longue date. .
Il faut bien entendu distinguer le problème d’une décompensation cétosique sur un mode insulinoprive d’un diabète où l’on enregistre un amaigrissement rapide et la présence d’une cétose.
2) Mise en route ambulatoire de l’insulinothérapie
La mise en route de l’insuline nécessite chez un patient pratiquant l’autosurveillance une consultation d’éducation à la technique d’injection.
Le moment de l’injection se fera en fonction de l’insuline choisie :
Avec l’insuline Detemir, l’injection se fait avant le repas du soir ou au coucher selon le schéma de l’insuline « Bedtime »
Avec l’insuline Glargine, on peut proposer au patient de choisir le moment de l’injection en maintenant la régularité de ce moment d’un jour sur l’autre.
Les injections sont faites de préférence dans les cuisses en variant quotidiennement le site d’injection afin d’éviter les lipodystrophies.
La longueur des aiguilles est fonction de la quantité d’insuline injectée ou de l’épaisseur du tissu sous cutané. L’injection se fait perpendiculairement à la peau avec ou sans pli cutané qui sera de toute manière large. Les aiguilles sont bien entendu à usage unique.
Dans la mise sous insuline ambulatoire, on démarre avec une dose faible que l’on augmente régulièrement en fonction de l’évolution glycémique.
3) Le suivi
L’autosurveillance
L’ajustement des doses d’insuline basale se fait en priorité sur le niveau glycémique à jeun. L’objectif est dans un premier temps d’amener la glycémie à jeun en dessous de 1,50 g/l puis dans un second temps, atteindre l’objectif optimal en dessous de 1,20 g/l.
On surveillera aussi avec intérêt la glycémie de fin de journée afin de dépister d’éventuelles hypoglycémies.
Les paramètres d’équilibre du diabète
La cible d’HbA1c est de 7% à ce stade du diabète que l’on ajustera selon l’âge et le niveau de retentissement.
Bien entendu, la prise en charge reste globale avec le contrôle du poids, le contrôle tensionnel, les éléments de protection rénale et cardiovasculaire intégrant le contrôle du bilan lipidique.
L’insulinothérapie dans le diabète de type 2 : quelques freins à lever
La peur des hypoglycémies : elle est à relativiser dans le diabète de type 2 car les patients gardent tout au long de leur diabète une résistance à l’insuline. L’augmentation progressive et encadrée des doses d’insuline et du patient permet de lever ce frein fréquent.
L’insuline, cela fait grossir : de base l’insuline est effectivement une hormone antilipolytique et lipogénétique. Elle favorise également l’anabolisme protéique et donc l’augmentation de la masse musculaire. Avec la mise sous insuline, il est souhaitable d’ajuster l’apport calorique pour prévenir une prise pondérale excessive. Un des facteurs les plus prédictifs de la prise de poids sous insuline est la disparition de la glycosurie qui représentait une « fuite d’énergie » par l’élimination urinaire de glucose.
En commençant l’insuline, je ne pourrai plus m’arrêter : c’est une réflexion fréquente chez nos patients qui pensent à une sorte de dépendance ou d’accoutumance au traitement. Ceci n’est bien entendu pas le cas mais l’insulinothérapie intervient à une phase évolutive de la maladie diabétique qui mérite d’être expliquée au patient. L’objectif n’est pas de mettre de l’insuline mais de prévenir les complications du diabète à un stade où le traitement oral ne suffit plus.
En conclusion :
L’insulinothérapie dans le diabète de type 2 s’inscrit dans l’histoire évolutive de cette maladie .Cette étape est souvent l’occasion d’une mise au point globale avec le patient dont l’adhésion et la motivation constituent des éléments primordiaux.
Références :
Haute Autorité de Santé : Recommandations professionnelles Traitement médicamenteux du diabète de type 2 Novembre 2006 www.has-sante.fr rubrique « Recommandations de bonne pratique »