Les tracas digestifs de la 1ère année du nourrisson.
Professeur Frédéric GOTTRAND
Hôpital Jeanne de Flandre
CHRU
59037 LILLE Cedex
Reflux gastro-oesophagien
Points forts :
- Une étude Française récente montre que la fréquence du RGO est de 32 % chez le nourrisson de moins de 1 an, 8% chez l’enfant de 1 à 11 ans et 11 % chez l’adolescent
- le RGO simple du nourrisson (se manifestant par des régurgitations isolées) ne nécessite ni examen complémentaire, ni prescription médicamenteuse
- L’endoscopie n’est justifiée qu’en cas de suspicion d’œsophagite et la pH-métrie pour le diagnostic de RGO occulte
- A part le cisapride dont l’utilisation est très restreinte chez l’enfant de moins de 3 ans, il n’y a pas de prokinétique efficace disponible actuellement. Les IPP ont montré une efficacité et obtenu une AMM pour l’œsophagite, la prévention des récidives d’œsophagite et le RGO symptomatique chez l’enfant de plus de 1an.
- Il existe un risque de prescription inappropriée et excessive des IPP chez l’enfant
Mots clés: reflux gastro-œsophagien, enfant, œsophagite, inhibiteur de la pompe à protons
Key words: gastro-esophageal reflux, children, oesophagitis, proton pump inhibitors
Le reflux gastro-œsophagien (RGO) est un phénomène physiologique défini par la remontée du contenu gastrique dans l’œsophage. Il est très fréquent chez le nourrisson, chez qui il se manifeste le plus souvent par des régurgitations (50% des nourrissons de 4-6 mois présentent au moins 3 régurgitations par jour). Le RGO est pathologique quand le reflux est responsable de symptômes gênants ou de complications (1).
Si les manifestations disparaissent dans la majorité des cas vers l’âge de 1 an, des signes peuvent persister toute l’enfance. Dans les cas non compliqués, aucun examen complémentaire n’est nécessaire (2).
Signes cliniques en fonction de l’âge.
La prévalence du RGO et les signes cliniques varient selon l’âge (tableau 1). Des régurgitations fréquentes (définie comme plus de 3 par jour) s’observent chez 20 à 30 % des nourrissons durant les premiers mois de vie. On estime que dans le monde 20 à 25 % des parents consultent au moins une fois un médecin pour des régurgitations du nourrisson. La fréquence des régurgitations varie largement en fonction de l’âge. Des régurgitations sont observées chez 50% des nourrissons de moins de 3 mois, chez plus de 66% des nourrissons à 4 mois, mais seulement chez 5% d’entre eux à l’âge de 1 an. Une étude longitudinale très récente confirme que 88% des régurgitations disparaissent à l’âge de 1 an (3). La disparition des régurgitations ne signifie cependant pas forcément que le RGO est guéri, et il existe actuellement des données montrant que le RGO peut chez certains enfants se prolonger plusieurs années, voire durant l’âge adulte, avec des manifestations différentes selon l’âge (tableau 1).
Diagnostic positif
Le diagnostic de reflux est habituellement clinique et les examens complémentaires ne doivent être proposés qu’aux enfants chez qui la clinique n’est pas évocatrice ou univoque. La pH-métrie de longue durée, réalisée actuellement le plus souvent en ambulatoire reste l’examen de référence pour le diagnostic de RGO. Chaque épisode de reflux acide est enregistré et il est possible par un marqueur d’événements sur le boîtier de corréler éventuellement la survenue d’un épisode de reflux à une manifestation clinique (toux, bradycardie, pleurs…). Un enregistrement prolongé d’au moins 18 heures est nécessaire pour interpréter l’examen de façon fiable. Il est alors possible de calculer des scores (pourcentage de temps passé à pH<4 sur temps total d’enregistrement définissant l’index de reflux qui est le critère le plus robuste de définition du RGO chez l’enfant) qui en comparaison avec des normes permettent le diagnostic du RGO acide et d’en mesurer l’importance. Cet examen doit être réalisé sans traitement antireflux pour faire le diagnostic de RGO. Il est parfois utile de le faire sous traitement prokinétique ou antisécrétoire quand il est nécessaire de savoir si le RGO persiste malgré le traitement, en vue d’une indication chirurgicale par exemple.
Le transit oeso-gastro-duodénal est un examen peu sensible et spécifique pour le diagnostic du RGO. Il présente cependant l’intérêt d’une accessibilité souvent plus grande que la pH-métrie et aussi de pouvoir mettre en évidence une malformation anatomique (rare) de l’œsophage ou de l’estomac.
En cas de suspicion d’œsophagite, l’endoscopie digestive haute permet d’affirmer ou d’éliminer le diagnostic voire d’évoquer un diagnostic différentiel (allergie, œsophagite à éosinophile…), par la réalisation de biopsies œsophagiennes et/ou gastriques. Cet examen ne fait pas le diagnostic du RGO mais de ses conséquences. Il permet de plus de faire le diagnostic de hernie hiatale, hernie par glissement chez l’enfant, et donc non visualisée habituellement par les examens radiologiques.
La place des autres examens (scintigraphie, manométrie, échographie, impédancemétrie œsophagienne) est beaucoup plus limitée en pratique (4).
Quelles sont les modalités thérapeutiques du RGO?
L’abstention. La majorité des nourrissons présentent des régurgitations simples, peu abondantes, qui disparaîtront spontanément avec l’âge. Les explications, la réassurance de la famille suffisent dans ces cas.
Les mesures diététiques et l’épaississement. La correction des erreurs diététiques (un nourrisson qui régurgite est souvent vorace et affamé, plus il régurgite plus il réclame et plus la famille est tentée d’augmenter les quantités… et donc d’auto-entretenir ce RGO) est la première mesure à entreprendre. L’épaississement peut être réalisé avec des laits épaissis (laits « confort » ou « AR ») à la caroube ou avec de l’amidon, ou alors des épaississants (Gumilk®, Gélopectose®) rajoutés dans le biberon. Les études réalisées avec les épaississants montrent clairement une efficacité sur le symptôme régurgitation, mais l’absence de toute efficacité sur le RGO par lui même (le nombre et la durée des reflux acides mesurés par pH-métrie ne sont pas modifiés). Les épaississants sont à tort considérés comme peu coûteux et anodins : des effets secondaires ont en effet été décrits : selles molles avec la caroube, ballonnements constipation avec l’amidon, bézoard gastrique, augmentation de la toux, quelques observations d’allergie à la caroube, effets potentiels sur l’absorption intestinale des nutriments, minéraux et oligoéléments.
Les prokinétiques. Le cisapride est le seul médicament prokinétique ayant démontré dans certaines études une efficacité sur le RGO chez l’enfant de moins de 3 ans. Quelques observations d’allongement du QT ont été rapportées chez des prématurés, pour des doses dépassant habituellement 0,8 mg/kg/j. Des cas d’allongement du QT et/ou de survenue de troubles du rythme ventriculaire (torsades de pointe) parfois mortels ont été rapportés (fréquence estimée à 2 pour 1 million de patients /mois), dans 85% des cas chez des patients adultes polymédiqués (recevant des inhibiteurs du cytochrome P450 3A4) et/ou porteurs d’une pathologie cardiaque préexistantes ou d’autres facteurs de risque favorisant les troubles du rythme. Actuellement son utilisation est très limitée, aux enfants de moins de 3 ans après échec des autres traitements du RGO. La prescription doit être faite par un pédiatre hospitalier après réalisation d’un bilan sanguin et d’un électrocardiogramme, répétés 72 heures après l’instauration du traitement, et la délivrance du cisapride est faite par rétrocession par les pharmacies hospitalières (depuis août 2005). Pour les autres prokinétiques disponibles actuellement (dompéridone et métoclopramide), aucune étude n’a pu démontrer leur efficacité par rapport au placebo. Le métoclopramide est un médicament difficile à utiliser compte tenu de la fréquence de ses effets secondaires et l’étroitesse de la marge entre dose efficace et dose toxique. Le dompéridone du fait de sa bonne tolérance, et malgré l’absence de preuve de son efficacité est ainsi redevenu le médicament de première intention du RGO chez l’enfant.
Les anti-acides n’ont pas d’efficacité directe sur le RGO mais sur l’œsophagite, et donc sur certains symptômes comme le pyrosis. Les effets secondaires les plus habituels sont des troubles du transit ; ils peuvent interagir avec l’absorption de certains médicaments, et exposer à une intoxication par l’aluminium en cas d’utilisation très prolongée et d’insuffisance rénale.
Les antisécrétoires sont représentés par les anti-H2 (cimétidine, ranitidine, famotidine, nizatidine) et les inhibiteurs de la pompe à protons (IPP) (oméprazole, lanzoprazole, pantoprazole, rabeprazole, esomeprazole). Les données pharmacodynamiques et pharmacocinétiques sont encore rares chez l’enfant, sauf pour l’oméprazole, le pantoprazole (5) et l’esoméprazole (6) qui ont actuellement l’AMM en France en pédiatrie. Ils n’ont pas d’effet sur le RGO mais sur la sécrétion acide et donc sur le pyrosis et l’œsophagite. Les IPP ont très peu d’effets secondaires mais il existe encore peu de donnée sur leur utilisation au très long cours en pédiatrie (7, 8).
La chirurgie a des indications rares et bien codifiées. En pédiatrie c’est l’intervention de Nissen qui est la plus fréquemment réalisée.
Quelles indications ?
Un RGO chez un nourrisson sans signe d’œsophagite, de malaise ne s'explore pas, il est physiologique. Détecter la suralimentation, éviter les jus de fruits, mettre en place des mesures de puéricultures (tétine, éructation au cours des repas, bonne position, acheter des bavoirs, prendre patience…)
En cas de régurgitations gênantes utiliser des laits épaissis avant de penser médicaments.
Si les régurgitations persistent ou en cas de manifestations extra-digestives de RGO, la dompéridone peut être prescrite seule ou associée à des antiacides (habitude franco-française qui n’a jamais été réellement évaluée). En cas d’échec, le cisapride peut être prescrit après avis hospitalier spécialisé chez l’enfant de moins de 3 ans.
En cas de RGO symptomatique, les IPP (esoméprazole à partir de 1 an, pantoprazole à partir de 12 ans) peuvent être prescrits
En cas de signes d’œsophagite (douleurs ou malaise pendant le biberon, hématémèse, mauvaise croissance, pyrosis) une endoscopie est préférable avant traitement antisécrétoire. L’oméprazole et l’esoméprazole ont l’AMM dans cette indication en France chez l’enfant de plus de 1 an, le pantoprazole à partir de l’âge de 12 ans. Une autre position plus pragmatique est, en cas de signe clinique évoquant une œsophagite, de proposer un traitement d’épreuve par les antisécrétoires sans réaliser d’endoscopie préalable. Si cette attitude est retenue, il faut cependant en évaluer l’efficacité au bout de quelques semaines, remettre en cause le diagnostic en cas de non réponse au traitement (pratiquer alors une endoscopie ou évoquer un autre diagnostic, par exemple l’allergie aux protéines du lait de vache ou une œsophagite à éosinophiles), et en tout cas ne pas prolonger ce traitement plus d’un mois à 6 semaines.
L’utilisation au long cours des IPP dans le RGO de l’enfant n’est actuellement pas recommandée. Cependant dans des manifestations respiratoires ou ORL rattachées à un RGO, un traitement de quelques semaines à quelques mois par un IPP peut être discuté, compte tenu de l’absence actuelle d’alternative thérapeutique et de l’excellente tolérance habituelle de ces médicaments. Les risques sont de prescrire des IPP trop largement et de manière trop prolongée sans avoir fait un minimum d’investigations visant à établir l’existence du RGO et le bénéfice potentiel de ces médicaments.
La chirurgie est indiquée en cas de RGO sévère (œsophagite récidivante ou résistante, malaise grave résistant au traitement) ou de RGO du grand enfant dépendant du traitement médical.
Données épidémiologiques Françaises
Une étude épidémiologique descriptive observationnelle a récemment évaluée la prévalence du RGO chez les nourrissons, enfants et adolescents âgés de 0 à 17 ans, et décrit les symptômes ainsi que les mesures diagnostiques et thérapeutiques utilisées (9). Cette étude était réalisée auprès d’un échantillon de 584 médecins (404 médecins généralistes et 180 pédiatres), qui recensaient de façon systématique les enfants et adolescents de 0 à 17 ans vus en consultation durant les jours de recueil, et incluait un échantillon de 8279 consultations, représentatif des consultations pédiatriques françaises. Le diagnostic du RGO était laissé volontairement à la libre appréciation du médecin, afin d’obtenir une meilleure représentation de la réalité des pratiques, et en raison de l’absence de critères diagnostiques stricts du RGO de l’enfant (1). La fréquence du RGO est de 32 % chez le nourrisson de moins de 1 an, 8% chez l’enfant de 1 à 11 ans et 11 % chez l’adolescent, soit une prévalence de 10,3% sur l’ensemble de la population des moins de 18 ans en France (ce qui correspond à 1 406 525 enfants). Les régurgitations sont le symptôme le plus fréquent chez le nourrisson alors que le pyrosis est le signe principal chez le plus de 12 ans (tableau 2). Des examens complémentaires sont souvent pratiqués : la pH-métrie essentiellement chez les enfants de 1 à 11 ans (reflux occultes) alors que la fibroscopie est d’autant plus réalisée que l’enfant est plus âgé, près d’un tiers des adolescents ayant eu une endoscopie (tableau 2). Des traitements médicamenteux sont prescrits chez la quasi-totalité des enfants. Si on observe une diminution avec l’âge de l’utilisation des alginates/antiacides et des prokinétiques, à l’inverse il existe une augmentation avec l’âge de l’utilisation des IPP, près des 2/3 des adolescents présentant un RGO reçoivent un IPP (tableau 2).
Tableau 1 : Symptômes du RGO en fonction de l’âge
|
SIGNES |
NOURRISSON |
ENFANT |
ADULTE |
|
Régurgitation |
|
|
|
|
Vomissement |
|
|
|
|
Pyrosis |
? |
|
|
|
Douleur épigastrique |
? |
|
|
|
Douleur rétrosternale |
? |
|
|
|
Dysphagie |
? |
|
|
|
Pleurs fréquents / Irritabilité |
|
|
- |
|
Anémie / Melaena / Hematémèse |
|
|
|
|
Refus / Difficultés alimentaires / Anorexie |
|
|
|
|
Retard de croissance |
|
|
- |
|
Anomalies de posture / Syndrome de Sandifer |
|
|
- |
|
Hoquet persistant |
|
|
|
|
Erosions dentaires |
? |
|
|
|
Enrouement / Pharyngite |
? |
|
|
|
Toux chronique / Pneumopathie d’inhalation |
|
|
|
|
Wheezing / Laryngite / Otite |
|
|
|
|
Laryngomalacie / Stridor / Croup |
|
|
- |
|
Asthme / Sinusite |
- |
|
|
|
Sténose laryngée / Nodules cordes vocales |
- |
|
|
|
Malaise grave / Mort subite / Apnée / Désaturation |
|
- |
- |
|
Bradycardie |
|
? |
? |
|
Troubles du sommeil |
|
|
|
|
Altération de la qualité de vie |
|
|
|
|
Œsophagite |
|
|
|
|
Sténose œsophagienne |
- |
|
|
|
Barrett / Adénocarcinome de l’œsophage |
-/- |
/- |
/ |
Légende: très fréquent; fréquent; possible; ( ) rare; - absent; ? inconnu
Tableau 2 : Fréquence (%) des symptômes observés, des examens complémentaires réalisés et des traitements prescrits dans le RGO en fonction de l’âge en France (9)
|
Symptômes |
0 à 11 mois (n=588) |
1 à 11 ans (n=457) |
12 à 17 ans (n=203) |
|
Régurgitations |
88 *§ |
53 § |
33 |
|
Vomissements |
25 § |
31 § |
12 |
|
Pleurs/irritabilité |
46 |
20 |
- |
|
Pyrosis |
- |
21 |
86 * |
|
Examens complémentaires |
|
|
|
|
Fibroscopie |
7 |
14 £ |
30 £* |
|
pH-métrie |
9 |
24 £§ |
9 |
|
TOGD |
3 |
9 £§ |
3 |
|
Traitements prescrits |
|
|
|
|
Antiacides ou alginates |
72§ |
65 |
54 |
|
Prokinétiques |
67§ |
52§ |
25 |
|
IPP |
17 |
32£ |
64£* |
£ p<0,05 versus 1-11 mois
* p< 0,05 versus 1-11 ans
§ p<0,05 versus 12-17 ans
Conclusions
Le RGO est une pathologie fréquente motivant souvent un traitement médicamenteux et des examens complémentaires chez l’enfant. Chez le nourrisson, il importe de distinguer reflux physiologique/régurgitations simples et reflux pathologique. Les IPP sont efficaces sur l’œsophagite et les symptômes douloureux (chez les plus de 1 an) et bien tolérés. Leur prescription doit rester raisonnée et de courte durée.
Encadré sur douleur abdominales récurrentes
Comme pour l’adulte, les douleurs abdominales peuvent être classées en colon irritable, migraine abdominale, dyspepsie fonctionnelle et douleurs abdominales fonctionnelles (10). Les douleurs abdominales chroniques sont un motif très fréquent de consultation, en particulier à l’âge scolaire (concerne 10 à 15% des 5-10 ans). Si ces douleurs sont réelles (les enfants simulent rarement), la majorité de ces douleurs sont fonctionnelles (on considère qu’il y a moins de 10% d’étiologie organique). Les arguments en pratique en faveur d’une origine fonctionnelle sont l’âge supérieur à 3-4 ans, l’absence d’antécédent personnel ou familial, la normalité de l’examen clinique avec en particulier l’absence de retentissement sur la croissance staturo-pondérale, le caractère exclusivement diurne des douleurs dont le siège est periombilical sans irradiation, l’absence de signe d’accompagnement et le fait que les douleurs sont influencées par des facteurs extérieurs de stress (activité scolaire...). A l’inverse certains facteurs d’alarme sont en faveur d’une étiologie organique (tableau 3).
Faut-il faire des examens complémentaires ?
En dehors d’un point d’appel particulier ou de facteurs d’alerte pour une étiologie organique, aucun examen complémentaire n’est nécessaire. La répétition des examens complémentaires inutiles et potentiellement dangereux, risque de conforter la famille dans l’inquiétude d’un diagnostic qu’on n’arrive pas à poser et favorise le nomadisme médical et la course aux examens paracliniques (rappelons en particulier que la coloscopie et l’endoscopie digestive haute n’ont pas d’indication dans l’exploration de douleur abdominales d’allure fonctionnelle). Le recours à l’endoscopie digestive doit être restreint aux rares enfants présentant des signes d’œsophagite, gastrite ou ulcère (tableau 4).
Que faut-il faire en pratique ?
- Prendre son temps et écouter ( )
- Chercher des facteurs favorisants sous-jacents
- Eviter la course aux examens complémentaires
- Convaincre de l’anorganicité
- Ne pas nier le symptôme douleur ( )
- Encourager le sport et les activités d’éveil
- Ne pas « psychiatriser »
- S’aider parfois d’un « journal » de la douleur
- Peu (pas ?) de médicaments ( )
Tableau 3 : Signes d’alarme devant des douleurs abdominales chroniques de l’enfant (d’après (10))
Ø Douleur localisée dans le cadran supérieur ou inférieur droit
Ø Douleur réveillant l’enfant
Ø Dysphagie
Ø Arthrite
Ø Vomissement persistent
Ø Maladie prérirectale
Ø Hémorragie digestive
Ø Perte de poids involontaire
Ø Diarrhée nocturne
Ø Ralentissement de la croissance staturale
Ø Antécédent familial de maladie inflammatoire du tube digestif, de maladie cœliaque ou de maladie ulcéreuse
Ø Retard pubertaire
Ø Fièvre inexpliquée
Tableau 4 : Indications d’une endoscopie digestive haute devant des douleurs abdominales de l’enfant (11)
- Localisation épigastrique
- Sensibilité de la région épigastrique à la palpation
- Douleurs nocturnes
- Douleurs rythmées par l’alimentation
- Antécédents familiaux d’ulcère
- Perte pondérale
- Hémorragie digestive
- Nausées/vomissements
Références :
1. Sherman PM, Hassall E, Fagundes-Neto U, Gold BD, Kato S, Koletzko S, et al. A Global, Evidence-Based Consensus on the Definition of Gastroesophageal Reflux Disease in the Pediatric Population. Am J Gastroenterol 2009.
2. Gottrand F. [Gastroesophageal reflux in childhood]. Arch Pediatr 2006;13(7):1076-9.
3. Campanozzi A, Boccia G, Pensabene L, Panetta F, Marseglia A, Strisciuglio P, et al. Prevalence and natural history of gastroesophageal reflux: pediatric prospective survey. Pediatrics 2009;123(3):779-83.
4. van Wijk MP, Benninga MA, Omari TI. Role of the multichannel intraluminal impedance technique in infants and children. J Pediatr Gastroenterol Nutr 2009;48(1):2-12.
5. Tolia V, Bishop PR, Tsou VM, Gremse D, Soffer EF, Comer GM. Multicenter, randomized, double-blind study comparing 10, 20 and 40 mg pantoprazole in children (5-11 years) with symptomatic gastroesophageal reflux disease. J Pediatr Gastroenterol Nutr 2006;42(4):384-91.
6. Gilger MA, Tolia V, Vandenplas Y, Youssef NN, Traxler B, Illueca M. Safety and tolerability of esomeprazole in children with gastroesophageal reflux disease. J Pediatr Gastroenterol Nutr 2008;46(5):524-33.
7. Tolia V, Boyer K. Long-term proton pump inhibitor use in children: a retrospective review of safety. Dig Dis Sci 2008;53(2):385-93.
8. Hassall E, Kerr W, El-Serag HB. Characteristics of children receiving proton pump inhibitors continuously for up to 11 years duration. J Pediatr 2007;150(3):262-7, 267 e1.
9. L Martigne L, Delaage PH, Thomas-Delecourt F, Barthélemy P, Gottrand F. Prévalence du reflux gastro-œsophagien (RGO) chez l’enfant et l’adolescent en France : résultats d’une étude observationnelle transversale. Gastroentérol Clin Biol 2009;33(Hors Série 1):P-43.
10. Rasquin A, Di Lorenzo C, Forbes D, Guiraldes E, Hyams JS, Staiano A, et al. Childhood functional gastrointestinal disorders: child/adolescent. Gastroenterology 2006;130(5):1527-37.
11. Mougenot JF, Faure C, Olives JP, Chouraqui JP, Codoner P, Gottrand F, et al. [Recommendations of the French Hepatology, Gastroenterology and Pediatric Nutrition Group. Current indications for digestive system endoscopy in children]. Arch Pediatr 2002;9(9):942-4.
LA CONSTIPATION DE L'ENFANT
La constipation est une pathologie très fréquente en pédiatrie, représentant 3% des consultations de pédiatrie générale et jusqu’à 25% des consultations de gastro-entérologie pédiatriques (1). La constipation est d’origine le plus souvent fonctionnelle et son diagnostic repose sur l’examen clinique dans la majorité des cas.
Ses circonstances de découvertes peuvent cependant être variées et non spécifiques, faire errer le diagnostic et ainsi exposer l’enfant à des examens complémentaires ou des traitements inutiles et potentiellement néfastes. A l’inverse, le risque peut être parfois de poser à tort ce diagnostic de facilité, et d’ainsi laisser évoluer une pathologie organique sous-jacente.
Classiquement le diagnostic de constipation peut être porté devant la présence d’au moins 1 des 3 critères suivants :
- rareté des exonérations : < 2 selles par jour chez l’enfant nourri au sein
< 3 selles par semaine chez l’enfant de moins de 3 ans
< 2 selles par semaine chez l’enfant plus grand
- dureté des selles
- difficultés d’émission des selles
Il ne faut donc pas se limiter à la fréquence des selles : un enfant émettant plusieurs selles dures quotidiennes présente ainsi une authentique constipation.
Les signes plus trompeurs sont :
- douleurs abdominales chroniques ou récurrentes
- douleurs abdominales aiguës pouvant réaliser un tableau pseudo-appendiculaire
- pathologie anale : fissures anales, rectorragies, douleurs à la défécation, prurit anal, prolapsus rectal
- pseudo-diarrhée de stase
- encoprésie
- infections urinaires basses à répétition
La place des examens complémentaires doit rester limitée : ils sont le plus souvent inutiles, parfois coûteux, et potentiellement néfastes pour l'enfant - soit par leur risques propres (perforation colique par endoscopie par exemple) - soit par le risque d'organisation psycho-pathologique d'une pathologie fonctionnelle (manœuvres endo-rectales répétées par exemple). Ils ont cependant une place indiscutable dans certaines circonstances qui peuvent être schématiquement : 1- diagnostic positif d'une constipation quand la clinique et l'interrogatoire ne sont pas probants. 2- suspicion de pathologie organique, essentiellement maladie de Hirschprung. 3- analyse physiopathologique d'une constipation rebelle dans le but d'adapter la thérapeutique au type de constipation.
La radiographie d'abdomen sans préparation peut être utile au diagnostic de constipation quand la sémiologie n'est pas typique ou l'examen clinique difficile : enfant obèse ou opposé à l'examen ne permettant pas la palpation correcte de l'abdomen, ampoule rectale vide ou toucher rectal refusé par l'enfant. La radiographie d'abdomen sans préparation montre l'accumulation de matières fécales dans le colon, permet de localiser les fécalomes qui prédominent habituellement dans le recto sigmoïde, et permet parfois d'éliminer une pathologie organique (niveaux hydro-aériques en faveur d'un obstacle, spina bifida occulta, agénésie sacrée)(1). Elle permet de plus de juger de l'importance de l'accumulation des matières fécales et donc de la nécessité de lavements évacuateurs avant la mise en route d'une thérapeutique de fond. Elle permet également d'apprécier l'efficacité de la thérapeutique (lavements évacuateurs par exemple). La limite de cet examen est la subjectivité de son interprétation et la difficulté parfois de bien repérer les fécalomes, en particulier quand il existe des superpositions gazeuses importantes.
La mesure du temps de transit au carmin est un test simple, facile, qui permet d'authentifier la constipation sans préjuger de son mécanisme (2): il consiste en l'ingestion de 1 gramme de rouge carmin et la mesure du temps passé entre l'ingestion et la première selle rouge (normale <20h) et entre l'ingestion et la dernière selle rouge (normale <48h).
L'anuscopie est également un examen simple, indolore et utile pour rechercher une pathologie anale souvent associée à la constipation et dont la méconnaissance peut conduire à des échecs thérapeutiques ; sa réalisation ne doit pas être systématique mais guidée par la clinique (douleur à la défécation, rectorragie).
Par contre, la coloscopie n'a aucune indication dans la constipation de l'enfant. Le lavement baryté n'a pas non plus sa place dans la constipation habituelle de l'enfant, sauf quand certaines causes organiques sont suspectées (cf. infra). Il met souvent en évidence dans les constipations fonctionnelles un dolichomégacolon (3), simple conséquence de l'ancienneté du trouble mais sans incidence sur les choix thérapeutiques.
Les constipations organiques sont rares (moins de 5% des constipations de l'enfant (1)) mais de causes diverses. L'examen clinique est en général un bon élément d'orientation diagnostique que les examens complémentaires ne viennent que confirmer (bilan thyroïdien, calcémie...). Il convient néanmoins d'insister sur l'intérêt de réaliser au moindre doute sur une maladie de Hirschprung, une manométrie ano-rectale à la recherche du réflexe recto-anal inhibiteur; en cas d'absence de ce dernier, le diagnostic sera confirmé par une biopsie rectale qui reste le seul examen permettant de poser le diagnostic avec certitude, et l'étendue de la zone aganglionnaire appréciée par un lavement baryté. Les arguments anamnestiques et cliniques qui doivent faire suspecter une maladie de Hischprung et demander une manométrie ano-rectale sont: chez un garçon, constipation sévère de début précoce avec notion de retard d'émission du méconium, sans encoprésie, s'accompagnant d'un ballonnement abdominal, d'une ampoule rectale vide au toucher rectal avec épreuve à la sonde positive. Il faut cependant signaler des formes moins caricaturales pouvant par exemple se révéler après l’âge de 10 ans (4).
Quand une constipation persiste malgré un traitement symptomatique bien conduit pendant une période de 4 à 6 semaines (comprenant évacuation initiale des fécalomes, mesures hygiéno-diététiques, laxatif, et traitement de la fissure anale éventuelle), il devient alors nécessaire d'envisager des explorations fonctionnelles permettant d'apprécier le mécanisme physiopathologique de cette constipation et donc de lui apporter un traitement adapté. C'est la que prennent leur place l'étude du temps de transit segmentaire et la manométrie ano-rectale. L'étude du temps de transit se fait habituellement à l'aide de marqueurs radio-opaques ingérés 3 jours de suite avec réalisation à J4 et J7 d'une radiographie d'abdomen sans préparation (technique décrite par Chaussade (5), qui a l'avantage d'exposer à une faible irradiation et d'avoir été validée avec la technique de Ahran (6) et donc de pouvoir utiliser des normes pédiatriques françaises). Elle permet de distinguer les constipations de transit où les marqueurs radio-opaques s'accumulent dans le colon droit et le colon gauche, des constipations terminales où la rétention des marqueurs siège au niveau du recto-sigmoïde. La manométrie anorectale permet de préciser les anomalies dynamiques en cause dans les constipations terminales. La place de ces examens dans le suivi des patients est difficile à préciser; des guérisons cliniques avec persistances d'anomalies manométriques sont parfois observées; il semble cependant que la persistance de ces anomalies soit un facteur de risque de rechute (7). Quant à l'électromyographie, la manométrie colique et la défécographie, ils ne sont pas d'utilisation courante et leurs indications doivent rester réservées à des cas particuliers ou à des protocoles de recherche (8).
Si la constipation aiguë ou accidentelle répond habituellement bien (dans plus de 60% des cas) à des mesures hygiéno-diététiques et thérapeutiques simples (9), une évolution moins favorable est habituelle dans les constipations chroniques (10). L’éventail des mesures thérapeutiques est large, allant de la réassurance, associée à des mesures d’hygiène de vie simples (11) jusqu’à des techniques de rééducation par biofeed-back (12). Aussi, Une démarche clinique précise et rigoureuse doit permettre de restreindre la place des examens complémentaires dans la constipation de l'enfant et de guider au mieux la prise en charge thérapeutique.
Références :
1- V Loening-Baucke. Chronic constipation in children. Gastroenterology 1993, 105:1557-64.
2- SB Dimson. Carmine as an index of transit time in children with simple constipation. Arch Dis Child 1970, 45:232-5.
3- E Fourchy, MC Bretagne, M Schmitt, JC Hoeffel. Etude radiologique des constipations de l'enfant. La Médecine Infantile 1982,5:565-77.
4- D Turck, P Laffargue, F Gottrand, M Bonnevalle, MD Lamblin, P Debeugny, JP Farriaux. Révélation tardive de la maladie de Hirschprung chez l'enfant. A propos de 11 observations. Lille Méd 1988;28:178-80.
5- S Chaussade, H Roche, A Khyari, D Couturier, J Guerre. Mesure du temps de transit colique (TTC) : description et validation d'une nouvelle technique. Gastroenterol Clin Biol 1986; 10:385-9.
6- P Ahran, C Devroede, B Hehannin, M Lanza, C Faverdin, C Dornic, B Perzoz, M Tetreault, B Perey, D Pellerin. Segmental colonic transit time. Dis Colon Rectum 1981; 24:625-9.
7- V Loening-Baucke. Factors determining outcome in children with chronic constipation and faecal soiling; Gut 1989; 30:999-1006.
8- C Di Lorenzo, AF Flores, N Reddy, PE Hyman. Use of colonic manometry to differentiate causes of intractable constipation in children. J Pediatr 1992; 120:690-5.
9- FP Abrahamian, JD Lloyd-Still. Chronic constipation in childhood: a longitudinal study of 186 patients. J Pediatr Gastroenterol Nutr 1984; 3:460-7.
10- A Staiano, M Andreotti, L Greco, P Basile, S Auricchio. Long-term follow-up of children with chronic idiopathic constipation. Dig Dis Sci 1994;39:561-4.
11- RN van der Plas, MA Benninga, JAJM Taminiau, HA Büller. Treatment of defaecation problems in children: the role of education, demistification and toilet training. Eur J Pediatr 1997; 156:689-92.
12- RN van der Plas, MA Benninga, HA Büller, PM Bossuyt, LMA Akkermans, Redekop WK, JA Taminiau. Biofeedback training in treatment of childhood constipation: a randomised controlled study. Lancet 1996;348:776-80.
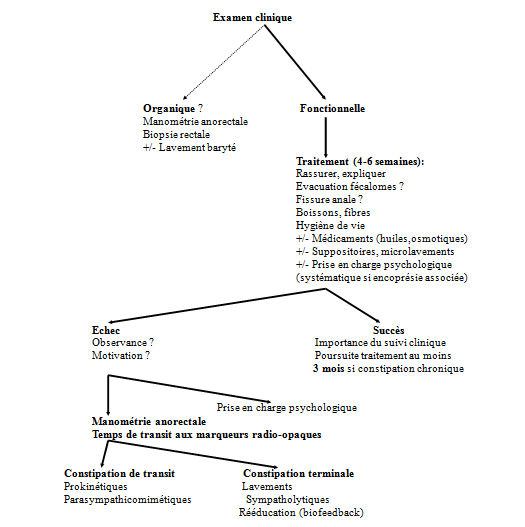
Constipation : proposition d’arbre décisionnel