Modalités du TSH de la ménopause
Docteur Geoffroy ROBIN
Geoffroy ROBIN, Hortense BAFFET, Brigitte LETOMBE
L’objectif du THM est, à court terme, de pallier les symptômes d’hypo-œstrogénie et notamment les bouffées de chaleur. Mais l’ensemble de ses effets va jouer sur l’amélioration de la qualité de vie des femmes ménopausées et sur leur bien être, en ralentissant l’ensemble du vieillissement des différents tissus. A plus long terme, le THM permet ainsi de lutter contre l’ostéoporose, d’améliorer les troubles trophiques ainsi que le profil lipidique des patientes.
Il est important de souligner, que malgré les critiques qui lui sont faites, le THM est le seul traitement ayant une action globale sur les modifications liées à la carence œstrogénique.
Le débat est constant quant au rapport bénéfice/risque du THM, avec des positions parfois discordantes entre les autorités de santé telles que l’AFSSAPS, l’Agence Européenne du médicament (AEM), et certaines sociétés savantes comme l’Association Française pour l’Etude de la Ménopause (AFEM) ou le GEMVI (Groupe d’Etude sur la Ménopause et le Vieillissement).
A) Composition du THM
Le principe de ce traitement est d’associer un œstrogène et un progestatif, ce dernier ayant pour fonction de s’opposer à l’effet proliférant des œstrogènes sur l’endomètre. En cas d’hystérectomie, il n’est donc pas nécessaire d’utiliser de progestatif.
Il existe de nombreux produits et voies d’administration des hormones contenues dans le THM, utilisables en France:
- Le 17β œstradiol est l’œstrogène naturel de référence et peut être utilisé par voie orale, percutanée (gel), ou transcutanée (patch) comme le montre le tableau 1.
Tableau 1 : Liste des œstrogènes disponibles en France
|
Voie d'administration |
Spécialité |
Dosage(s) |
Posologie |
Présentation |
|
Per os |
Estreva® |
1,5mg |
1/jour |
28 cp |
|
Per os |
Estrofem® |
1ou 2 mg |
1/jour |
28 cp |
|
Per os |
Oromone® |
1ou 2 mg |
1/jour |
28 cp |
|
Per os |
Progynova® |
1ou 2 mg |
1/jour |
20 ou 60 cp |
|
Per os |
Provames® |
1ou 2 mg |
1/jour |
30 ou 25 cp |
|
Percutanée |
Estreva® gel |
0,5 mg / pression |
1 à 3/jour |
gel |
|
Percutanée |
Oestrodose® |
0,75 mg / dose |
1 à 2/jour |
flacon |
|
Percutanée |
Oestrogel® |
1,5 mg /dose |
1/jour |
gel |
|
Percutanée |
Delidose® |
0,5 ou 1 mg /sachet |
1 à 2/jour |
sachet |
|
Transcutanée |
Oesclim® |
25/37,5/50/75/100 mg |
2 patch /semaine |
patch de 0,025 à 0,1 mg/24h00 |
|
Transcutanée |
Vivelledot® |
25/37,5/50/75/100 mg |
2 patch /semaine |
patch de 0,025 à 0,1 mg/24h00 |
|
Transcutanée |
Thais® |
25/50/100 mg |
2 patch /semaine |
patch de 0,025 à 0,1 mg/24h00 |
|
Transcutanée |
Estraderm® |
25/50/100 mg |
2 patch /semaine |
patch de 0,025 à 0,1 mg/24h00 |
|
Transcutanée |
Dermestril® |
25/50/100 mg |
2 patch /semaine |
patch de 0,025 à 0,1 mg/24h00 |
|
Transcutanée |
Climara® |
50 mg |
1 patch/semaine |
patch de 0,05 mg/24h00 |
|
Transcutanée |
Dermestril Septem® |
25/50/75 mg |
1 patch/semaine |
patch de 0,025 à 0,075 mg/24h00 |
|
Transcutanée |
Femsept® |
50/75/100 mg |
1 patch/semaine |
patch de 0,5 à 0,1 mg/24h00 |
|
Transcutanée |
Thais Sept® |
25/50/75 mg |
1 patch/semaine |
patch de 0,025 à 0,075 mg/24h00 |
|
Transcutanée |
Estrapatch® |
40/60/80 mg |
1 patch/semaine |
patch de 0,04 à 0,08 mg/24h00 |
Si les effets des œstrogènes sur les organes cibles sont identiques pour les diverses voies d’administration, les modifications métaboliques sont différentes et influenceront leur prescription. Car, il existe un effet de premier passage hépatique, lors de l’utilisation de la voie orale, induisant la synthèse de protéines hépatiques avec un effet métabolique délétère tel que la diminution de l’antithrombine III ou l’augmentation des triglycérides et des substrats de la rénine.
- Les progestatifs utilisables sont répartis en plusieurs groupes : la progétérone naturelle et son isomère la dydrogestérone ; les dérivés de la 17 OH progestérone (prégnanes) que sont l’acétate de chlormadinone, l’acétate de cyprotérone, la médrogestone et l’acétate de médroxyprogestérone et, enfin, les dérivés de la 19 norprogestérone (norprégnanes) que sont la promégestone et l’acétate de nomégestrol.
Comme le montre le tableau 2, ils sont tous utilisables par voie orale. Le choix du progestatif va dépendre de ses propriétés androgéniques, antiandrogéniques et glucocorticoïdes et donc de sa tolérance clinique.
Tableau 2 : Liste des progestatifs disponibles en France
|
Voie d'administration |
Classification |
Spécialité |
Dosage(s) |
Posologie |
Présentation |
|
Per os |
Progestérone |
Estima Gé® |
100 ou 200 mg |
1/jour |
15/30/45/90 cp |
|
Per os |
Progestérone |
Ménaelle® |
100 mg |
1/jour |
30 cp |
|
Per os |
Progestérone |
Utrogestan® |
100 ou 200 mg |
1/jour |
30 ou 15 cp |
|
Per os |
Dydrogestéronne |
Duphaston® |
10 mg |
1 ou 2/j |
10 cp |
|
Per os |
Acétate de Chloramdinone |
Lutéran® |
2/5/10 mg |
1/jour |
10 ou 12 cp |
|
Per os |
Acétate de Cyprotérone |
Androcur® |
50 mg |
1/jour |
20 cp |
|
Per os |
Médrogestone |
Colprone® |
5 mg |
1/jour |
20 cp |
|
Per os |
Acétate de Médroxyprogestérone |
Gestoral® |
10 mg |
1/jour |
14 cp |
|
Per os |
Acétate de Nomégestrol |
Lutényl® |
3,75 ou 5 mg |
1/jour |
14 ou 10 cp |
|
Per os |
Promegestone |
Surgéstone® |
0,125/0,25/0,5 mg |
1/jour |
10 ou 12 cp |
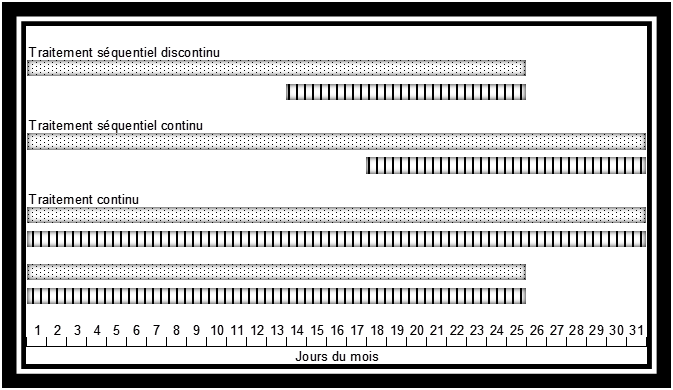
Plusieurs schémas de traitement existent et sont résumés dans la figure 1.
B) Les différents schémas de THM
1) Le schéma séquentiel
Il permet de restaurer des hémorragies de privation lors de l’arrêt du progestatif.
- Le schéma séquentiel discontinu consiste à donner un œstrogène, du 1er au 25ème jour du mois, auquel est associé un progestatif au moins 12 jours, c'est-à-dire du 14ème au 25ème jour du mois.
- Le schéma séquentiel continu consiste à poursuivre les œstrogènes, du 1er au 31ème jour du mois, en association avec un progestatif, en général 14 jours au moins, c'est-à-dire du 18ème au 31ème jour du mois.
2) le schéma continu
La prise continue d’un œstrogène, associé à un progestatif pour la même durée, induit une atrophie endométriale, supprimant les hémorragies de privation. Cette prise peut se faire du 1er au 25ème jour du mois avec un arrêt de 5 jours ou du 1er au 31ème jour du mois, c'est-à-dire une prise ininterrompue. Ce traitement convient surtout aux femmes ménopausées depuis au moins 2 ans. En effet, s’il est débuté avant, une augmentation de risque de saignement intercurrent est possible.
Figure 1 : les différents modes d’administration du THM
3) les THM « prêts à l’emploi »
Il existe certaines spécialités de THM, dites « prêtes à emploi », c'est-à-dire combinant un œstrogène et un progestatif dans un même comprimé, utilisables dans ces deux modes de schémas thérapeutiques comme le montre le tableau 3.
Tableau 3 : liste des THM « prêts à emploi » disponibles en France en 2010 (Vital 2010)
|
Schéma |
Voie d'administration |
Spécialité |
Dosage(s) |
Présentation |
|
Séquentiel |
Per os |
Climaston® 1/10 |
1 mg d'E2 10 mg Dydrogestérone (14j) |
28 cp sans arrêt |
|
|
Per os |
Climaston® 2/10 |
2 mg d'E2 10 mg Dydrogestérone (14j) |
28 cp |
|
|
Per os |
Climène® |
2 mg valérate E2 1 mg Acétate Cyprotérone (10j) |
21 cp |
|
|
Per os |
Divina® |
2 mg valérate E2 10 mg Acétate Médroxyprogestérone (10j) |
21 cp |
|
|
Per os |
Trisequens® |
1 ou 2 mg valérate E2 1 mg Acétate Noréthindrone (10j) |
28 cp sans arrêt |
|
|
Per os |
Novofemme® |
1 mg d'E2 1 mg d'Acétate de Noréthistérone |
28 cp sans arrêt |
|
|
Per os |
Naemis® |
1,5 mg d'E2 3,75 mg Acétate Nomégestrol (14j) |
24 cp |
|
|
Patch |
Femsept combi® |
1,5 mg d'E2 1,5 mg Lévonorgestrel |
1 patch/semaine |
|
Continu |
Per os |
Activelle® |
2 mg d'E2 1 mg Acétate Noréthindrone |
28cp |
|
|
Per os |
Climaston® 2/5 |
2 mg d'E2 5 mg Dydrogestérone (14j) |
28 cp |
|
|
Per os |
Kliogest® |
2 mg d'E2 1 mg Acétate Noréthindrone |
28 cp |
|
|
Per os |
Angeliq® |
1mg d'E2 2 mg Drospirénone |
28 cp |
|
|
Per os |
Duova® |
1 ou 2 mg d'E2 2,5 ou 5 mg Acétate Médroxyprogestérone |
28 cp |
|
|
Patch |
Femseptevo® |
1,5 mg d'E2 0,525 mg Lévonorgestrel |
1 patch/semaine |
C) Indications du THM
L’AFSSAPS [8] stipule que le THM est indiqué chez les femmes ayant des troubles du climatère suffisamment gênant pour altérer leur qualité de vie. Dans ce cas, le traitement peut être instauré, si la femme le souhaite, à dose minimale et pour une durée la plus courte possible, mais tant que persistent les signes de carence œstrogénique. D’un point de vue médicolégal, à ce jour, aucune durée limitée de l’utilisation du THM n’a été établie. Ainsi, les doses d’œstrogènes et de progestatifs constituant le THM seront débutées aux posologies les plus basses et augmentées progressivement jusqu’à obtenir la cessation des symptômes.
Toutefois, à l’instauration du traitement, l’AFSSAPS rappelle que les patientes doivent être clairement informées des risques inhérents à ce traitement.
D) Contre-indications du THM
Le dernier rapport de l’AFSSAPS, datant de 2006, souligne que le THM est contre-indiqué dans les situations suivantes :
- la présence d’hémorragie génitale sans diagnostic établi,
- un accident thrombo-embolique artériel ou veineux récent (> 2ans) ou en évolution,
- un antécédent de thrombose veineuse à répétition ou une thrombophilie connue qui n’est pas sous traitement anticoagulant,
- une affection hépatique aiguë ou chronique, ou des antécédents d’affection hépatique, jusqu’à la normalisation des tests hépatiques,
- l’hypersensibilité aux principes actifs ou à l’un des excipients contenus dans le THM,
- un cancer du sein connu ou suspecté ou autres néoplasies œstrogénodépendantes.
Il existe des affections devant faire évaluer la balance bénéfice/risque avant l’instauration du traitement :
- un antécédent de certaines tumeurs oestrogéno-dépendantes, telles l’adénocarcinome du col utérin, les carcinomes endométrioides ovariens ou le mélanome cutané,
- la présence de myome utérin, d’endométriose, ou un antécédent d’hyperplasie endométriale,
- une mastopathie fibro-kystique,
- un antécédent thromboembolique ou la présence de facteurs de risque,
- la présence de facteurs de risque cardiovasculaire, tels une HTA, un diabète, une hypercholestérolémie, une obésité, un tabagisme,
- la présence d’affections hépatiques, telles que les porphyries ou les adénomes hépatiques,
- les migraines.
E) Surveillance et adaptation du traitement
La surveillance d’une femme sous THM, doit être régulière et consiste en un examen clinique au moins annuel comprenant un interrogatoire à la recherche de signes d’hyper ou d’hypo-œstrogénie ou de l’existence de métrorragies, accompagné d’une palpation mammaire minutieuse et d’un examen gynécologique complet.
L’adaptation du traitement se fait essentiellement grâce à la clinique. Le praticien s’attachera à détecter :
- les signes d’hypo-œstrogénie persistants, tels que la reprise des bouffées de chaleur, la sécheresse vaginale, les troubles du sommeil, l’asthénie… traduisant la nécessité de rétablir une balance œstro-progestative en faveur d’une plus grande concentration œstrogénique.
- les signes d’hyper-œstrogénie, tels que les mastodynies, la sensation de gonflement, la prise de poids signant un surdosage en œstrogène.
La surveillance sénologique est indispensable par :
- Palpation mammaire annuelle
- mammographie bilatérale tous les 2 ans, complétée parfois d’une échographie mammaire.
L’existence de métrorragies, doit faire réaliser une biopsie d’endomètre et une échographie pelvienne à la recherche d’une hyperplasie endométriale ou d’un carcinome de l’endomètre. On estime, à l’échographie, que si l’épaisseur endométriale est inférieure à 8mm sous THM, le risque de cancer de l’endomètre est quasi nul.
La masse osseuse peut être appréciée par la réalisation d’une ostéodensitométrie, notamment chez les femmes à haut risque d’ostéoporose. Le risque fracturaire est significatif au-delà d’une déviation standard de -2DS sur le T-Score.
Un bilan métabolique avec dosage de la glycémie et des lipides est à effectuer régulièrement (pas de consensus sur le rythme de surveillance des paramètres métaboliques).
Il convient d’évaluer de façon régulière la balance bénéfice/risque liée au traitement. Notamment, les suspensions temporaires de traitement permettront d’évaluer la persistance de bouffées de chaleur nécessitant une poursuite du traitement alors que leur disparition lors de cette fenêtre d’interruption thérapeutique de plusieurs semaines, imposera l’arrêt définitif du traitement.
Pour en savoir plus :
- Postmenopausal Hormonal Therapy: An Endocrine Society Scientific Statement. JCEM 2010; 95(7) suppl1.
- ROZENBAUM H. La ménopause. Edition ESKA ; 2008.
- AFSSAPS. Mise au point actualisée sur le traitement hormonal de la ménopause (THM) 2006. Disponible sur <http://www;afssaps.santé.fr>
- ROZENBAUM H. Traitement Hormonal Substitutif. Ménopaurama AFEM 2003. Disponible sur <htpp://menopauseafem.com>